|
|
Расщепление пептидной и сложноэфирной связиБез участия фермента в водной среде. Как сказано в эпиграфе любое химическое превращение определяется прежде всего разрывом определенных химических связей. Молекулярные ножницы разрезают химические связи весьма эффективно и при том «в нужном месте и в нужное время». Реакция разрыва химической связи в молекуле А — В (не обязательно двухатомной) на части А и В может происходить в жидкой среде, когда молекула сталкивается с молекулами растворителя. Но этот процесс является маловероятным. Сначала поясним это на примерах разрыва пептидной связи (ПС) в белковой молекуле и сложноэфирной связи в молекуле нейромедиатора ацетилхолина (АХ), находящихся в воде при комнатной температуре. Затем рассмотрим, как эффективно “режут” эти связи молекулы-ножницы (гидролитические ферменты). В процессе пищеварения ПС должны быть разорваны и белковые цепочки расщеплены до аминокислот, которые и попадают в кровь и доставляются с кровотоком ко всем клеткам организма. “Разрезание” сложноэфирной связи в молекуле ацетилхолина с образованием холина и ацетата непрерывно должно происходить в межклеточном пространстве нейронов для поддержания нормального функционирования нервной системы. Мы выбрали эти типичные и вместе с тем замечательные ферменты потому, что их строение (геометрия) в кристаллическом состоянии хорошо известны. Достаточно хорошо изучены также и химические превращения в фермент-субстратном комплексе (ФСК) внутри активного центра (АЦ) этих ферментов. Реакция разрыва пептидной связи может происходить в водном растворе белка. Однако, это очень медленный процесс. Он осуществляется по следующей схеме:

Здесь R1, R2 — остатки двух соседних аминокислот фрагмента пептидной цепи, ПС между которыми (показана волнистой чертой) подлежит разрыву. Более подробно эта реакция записывается следующим образом:
Здесь ПК означает промежуточный комплекс. Такой ПК образуется с участием ионов гидроксила Реакция гидролиза АХ с образованием холина (ХОН) и ацетата
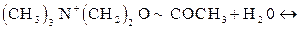
или
Заметим, что АХ и продукты его гидролиза Х Пользуясь выражением для скорости разрыва связи (или образования продукта Р), напишем общую формулу:
Здесь Е — энергия разрываемой связи, [Р] и [OH-] — концентрации продукта и гидроксила. Фактор 1/n, называемый “энтропийным”, является вероятностью того, что атака и сорбция [OH-] произошла “в нужном месте”. Фактор kбT/h определяет среднее число тепловых флуктуаций на разрываемой связи, а m0 зависит от времени сорбции [OH-]. Положим
где DS=-kб ln n. Тогда “абсолютная скорость” запишется в виде:
Здесь F=E-TDS — свободная энергия разрыва связи. Сделаем некоторые оценки. Пусть T=300 K, kT=0,6 ккал = 0,025 эВ = =4 10-13 эрг. Тогда kб T/h=4 1013 Гц. Если положить m0 ~1, то из (1.19) и (1.20) видно, что основной вклад в скорости процессов вносят экспоненциальные множители. Напомним, что для химической связи Е ~100 kб T! Рассмотрим следующую таблицу, показывающую, как зависит Kабс от величины F:
Что бывает, если вместо [OH-] в качестве катализатора выступает фермент? Его роль сводится прежде всего: 1) к изменению энтропийного фактора 1 /n=exp (T D S/kбT); 2) понижению энергетического барьера D Е. При этом для разрыва связи кроме энергии тепловых флуктуаций и энергии сорбции не требуется какого-либо другого источника энергии. Иногда говорят, что большая и сложная молекула фермента представляет собой “структурированный растворитель” для субстрата, который может образовать с молекулой субстрата фермент-субстратный комплекс. Вспоминая слова эпиграфа, можно сказать, что молекула А — В попадает в специально организованное силовое поле и фиксируется в нем. При этом параметры потенциального рельефа все время флуктуируют. Отдельные заряженные колеблющиеся атомы или группы атомов АЦ фермента играют роль гидроксильной группы, которая работает в водном растворе. Потенциальный рельеф в кармане АЦ организован специальным образом: в образовавшемся ФСК величины Е (и D F) снижаются. Атаки разрываемой связи заряженными группами происходят не беспорядочно, как в воде со стороны ОН-, а по фиксированным направлениям. Ниже приводиться разбор физических основ последовательных этапов работы молекулярных ножниц на примере АХТ.
  ЧТО ПРОИСХОДИТ ВО ВЗРОСЛОЙ ЖИЗНИ? Если вы все еще «неправильно» связаны с матерью, вы избегаете отделения и независимого взрослого существования...  Система охраняемых территорий в США Изучение особо охраняемых природных территорий(ООПТ) США представляет особый интерес по многим причинам...  Что будет с Землей, если ось ее сместится на 6666 км? Что будет с Землей? - задался я вопросом...  Что способствует осуществлению желаний? Стопроцентная, непоколебимая уверенность в своем... Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
|